|
Una correcta interpretación de los
datos P-T estimados en una roca necesita de una evaluación de la
incertidumbre inherente a los cálculos. Esta incertidumbre resulta de la
propagación de los errores asociados a los distintos parámetros que
deben conocerse para solucionar la ecuación (49) para P o T. Por tanto,
dependiendo de la exactitud con la que se conozcan los parámetros
anteriores así será la incertidumbre de una estimación de P o T. La
transmisión de errores ha sido considerada más arriba de manera
cualitativa, al evaluar el efecto del error en la estimación de Keq
sobre los cálculos de temperatura (a P constante) en reacciones con
entalpías de reacción contrastadas.
No se pretende aquí revisar en detalle
el cálculo de errores propagados, que ha sido tratado en sus diversos
aspectos por Powell (1985), Hodges y Crowley (1985), Hodges y McKenna
(1987), McKenna y Hodges (1988), Kohn y Spear (1991a y b) y Powell y
Holland (1985, 1988, 1994). El objetivo a cubrir es ofrecer una visión
general de los factores que controlan la incertidumbre en las
estimaciones termobarométricas, y presentar algunos cálculos sencillos.
Las fuentes de incertidumbre inherentes
a los cálculos termobarométricos son:
-
Errores en las propiedades
termodinámicas de reacción.
-
Imprecisiones en la determinación
de la composición mineral.
-
Imperfecciones en los modelos de
solución, debido al conocimiento muy limitado del comportamiento de
las soluciones sólidas.Heterogeneidad composicional debida
a la ausencia de equilibrio perfecto.
-
Errores en las estimaciones
independientes de temperatura (para barómetros) y de presión (para
termómetros).
La estimación de los errores en las propiedades termodinámicas de reacción depende del método por el
cual se calculen las mismas. Las propiedades termodinámicas de reacción
pueden obtenerse directamente, a partir de calibrados experimentales o
empíricos de la reacción como los presentados más arriba. En este caso,
los métodos de regresión permiten obtener estimaciones del error en los
incrementos de entalpía y entropía de reacción (el incremento de volumen
de reacción se debe conocer previamente). Generalmente, el error en la
entalpía de reacción es el más elevado. Alternativamente, las
propiedades termodinámicas de reacción pueden calcularse a partir de las
propiedades de las fases puras. De nuevo, la entalpía molar es la
propiedad peor conocida, ya que se determina a partir de experimentos de
calorimetría, o mediante métodos de regresión sobre datos experimentales
de equilibrios de fases (i.e., bases de datos internamente consistente).
En cambio, el volumen molar puede determinarse con bastante precisión a
partir del volumen de la celdilla unidad obtenido mediante estudios de
difracción de RX. Así mismo, la entropía molar también puede conocerse
con bastante precisión, ya que su componente térmico (entropía de la
tercera ley) se obtiene del conocimiento de la capacidad calorífica, que
puede estimarse con bastante exactitud, y su componente configuracional,
de existir es estimable con métodos de difracción de RX. Los errores en
las propiedades termodinámicas pueden considerarse pequeños en el caso
de bastantes fases puras comunes que han sido profusamente estudiadas.
Las bases de datos termodinámicos suelen ofrecer los errores asociados a
estas propiedades. En general, la incertidumbre en el cálculo de T y P
debido a los errores en las propiedades termodinámicas de reacción es
mayor de unas decenas de grados y unas centenas de bares.
Los errores en la estimación de la composición mineral derivados de defectos en la instrumentación
analítica pueden ser importantes en algunos casos (e.g., calibración
defectuosa), aunque generalmente son pequeños para los elementos mayores
de las fases (<±2% relativo) debido a la excelente reproducibilidad de
aparatos tales como la microsonda electrónica. Sin embargo, el error en
el cálculo de la fórmula estructural, necesaria para evaluar las
proporciones molares de los componentes, puede ser elevado si no se
dispone de análisis completos en fases de hierro e hidratadas. Esta
fuente de error es común debido a que la mayor parte de los análisis se
obtienen actualmente con microsonda electrónica, que no permite una
estimación independiente de Fe3+, Fe2+ y H+.
Las imperfecciones de los modelos de
solución
disponibles para las soluciones sólidas constituyen la fuente de error
más importante en las estimaciones termobarométricas en rocas. En
apartados precedentes hemos tenido ocasión de comprobar la fuerte
dispersión en los resultados termobarométricos que resultan de la
consideración de distintos modelos de solución (Figura 10).
En este sentido Holland y Powell (1990, p.110) señalan:
“...geobarometry
is less precise than its practitioners would have us believe, and
the problem usually lies not with the calibrations or with the
thermodynamic data used for the equilibria but with poorly-known
activity-composition relations for the end-members in the mineral
phase”.
Este error es difícilmente
cuantificable, debido a la dificultad en la descripción del
comportamiento energético de soluciones sólidas complejas. Incluso en
soluciones sólidas relativamente simples y que han sido muy estudiadas,
como el granate, los errores debidos a las imperfecciones de los modelos
de solución son elevados. Como indican Koziol y
Newton (1989, p. 423):
"An error in
the activity coefficient of a garnet component, specially a dilute
component such as grossular or pyrope in garnets from pelitic rocks,
can make a large difference in the calculated activity of that
component, which translate into sizable errors in the calculated
temperatures and pressures of recrystallization of natural
assemblages".
Añadido en septiembre de 2022 al respecto de
la incertidumbre en los cálculos de pseudosecciones (o diagrama de asociaciones
de fases, fijando la composición del sistema = roca).
Recientemente, Richard White (https://www.st-andrews.ac.uk/earth-sciences/people/rww3)
escribió en la lista de correo Geometamorphism lo siguiente:
"I would argue that there remains significant uncertainties in constraining peak conditions in granulites and all other facies. We have hopefully reduced the uncertainties but they have not gone. Quantitative Phase petrology is a powerful tool that has allowed us to improve our understanding of many aspects of metamorphism, in particular things like melting, and stable assemblage relationships but predicted stability fields do have significant uncertainty associated with the thermodynamic models, and as they are fields there is a substantial uncertainty associated with their size. Approaches such as compositional isopleth intersections are in essence prone to some of the same pitfalls as conventional thermometry. While it is a convenient untruth to take these calculations as an absolute correct answer and assume that those who produce a-x models have got then perfectly correct, or even just
mildly inaccurate, the inconvenient truth is rather different."
Y Matt Kohn (https://www.boisestate.edu/earth/staff-members/matthew-j-kohn/)
escribió lo siguiente:
"Have uncertainties in thermodynamic database predictions ever been calculated? Yes, Roger Powell and Tim Holland have talked about this, but I think they always include an uncertainty in activity models. So, the inherent error in the database has not been evaluated independently. Error propagation for thermobarometers (e.g., Kohn and Spear, 1991; Am Min) indicates activity models can be a major contributor to uncertainty. And although our understanding of some minerals has improved a lot (garnet, plagioclase), which improves thermobarometry, the stability fields on a mineral assemblage diagram depend on all minerals in a database. So, errors in minerals like amphiboles, which might not affect your favorite thermometer, do propagate to errors in predicted assemblages."
En fases más complejas (e.g., biotita,
piroxenos, anfíboles), este tipo de error es mucho más importante, ya
que los modelos de solución disponibles aplican en sistemas simples,
esto es, cuando las fases presentan un número limitado de componentes, y
en no pocos casos se recurre a la consideración de comportamiento ideal
(e.g., como hemos visto anteriormente para la biotita en el termómetro
GARB).
El error debido al grado de heterogeneidad composicional en las fases es el resultado del grado
de equilibrio que presente la roca. Dejando aparte las zonaciones
minerales progradas, estas heterogeneidades composicionales se
desarrollan generalmente en fases que se reequilibran con facilidad
durante la sección retrógrada de la trayectoria P-T (e.g., biotita).
Como se ha indicado previamente, en estos casos no existe garantía de
que las composiciones seleccionadas representen composiciones de
equilibrio. Es necesario por tanto realizar análisis detallados de la
heterogeneidad composicional, para deducir posibles composiciones
equilibradas en estadios sucesivos. La magnitud de este error depende de
la heterogeneidad composicional, y en consecuencia, de la historia
metamórfica de la región estudiada y de la selección de las muestras. En
algunos casos, como en las unidades alpujárrides de las zonas internas
de las Cordilleras Béticas, esta fuente de error es la más importante
(García-Casco, 1993).
Finalmente, el error en las estimaciones independientes de T (para barómetros)
y de P
(para termómetros) puede ser importante dependiendo de los equilibrios
(o métodos alternativos) de estimación. Si se utilizan equilibrios de
fases, la estimación de estos errores es complicada, ya que todos los
equilibrios son en mayor o menor medida dependientes de P y T. En
consecuencia, estamos ante un ciclo irresoluble: no puede conocerse P
sin conocer previamente T, y para ello debemos conocer P. Esta situación
se resuelve si la técnica termobarométrica utilizada es la solución
simultánea de dos equilibrios. La intersección define de manera
única la temperatura a la que debe calcularse el barómetro y la presión
a la que debe calcularse el termómetro, lo cual permite estimar los
errores de P y T en la intersección.
De esta breve consideración, puede
concluirse que la segunda y tercera fuentes de error enumeradas son las
más importantes en la mayor parte de los casos prácticos,
particularmente si las asociaciones de fases se acercan al equilibrio.
La ecuación básica de transmisión de
errores estadísticos es:
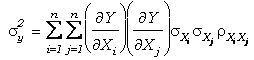 (104)
(104)
donde Y es la
variable dependiente para la que calculamos el error propagado, Xi(=1..n)
y Xj(=1..n) son las variables independientes de Y (Y=f(X1,X2,...Xn)),
sXi y
sXj son
las desviaciones estándar (i.e., error) de las variables independientes
Xi
y Xj, y rXiXj
es el coeficiente de correlación entre Xi y Xj.
Consideremos como ejemplo el error
transmitido en la estimación de T mediante un termómetro. Partiendo de
la ecuación termométrica general simplificada (50):
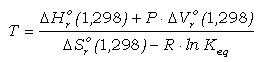 (50)
(50)
donde se asume
que DCpr=Dar=Dbr=0,
apreciamos que T es una función de 5 variables (R es constante y sin
error). La expansión de la ecuación (104) considerando errores en las
cinco variables, y notando que
rXiXi=1, resulta en:

que agrupando términos queda:
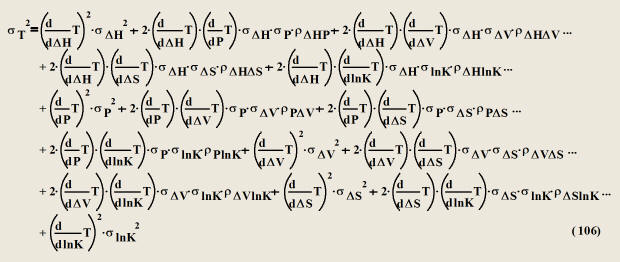
Teniendo en cuenta que las derivadas
parciales de la función de temperatura son:
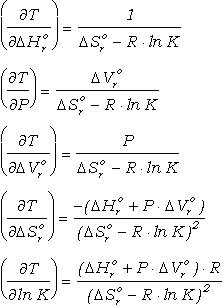 (107)
(107)
y disponiendo
de estimaciones para sXi
y
rXiXj,
pueden obtenerse las soluciones para el error transmitido en la
estimación de temperatura. Como puede suponerse, esto no es un problema
sencillo, pero la ecuación de transmisión de error puede simplificarse
considerablemente si consideramos que las variables no muestran
correlación alguna, ya que entonces (rXiXj)i¹j=0.
En este caso, la ecuación resultante es:
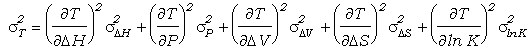 (108)
(108)
Aunque en el
caso más general las variables termodinámicas
DHro(1,298),
DSro(1,298)
y DVro(1,298)
presentan correlaciones distintas de cero,
la ecuación (107) puede asumirse como una aproximación aceptable.
La estimación de la incertidumbre en
los incrementos de las propiedades termodinámicas se puede obtener
directamente de los estudios experimentales de calibración de los
equilibrios, o a partir de las bases de datos internamente consistentes.
La incertidumbre en la presión suele asumirse en función de la exactitud
con la que se crea se ha estimado. En general, puede considerarse en
torno a ±1kbar. La estimación de
slnK es
más complicada, ya que debe realizarse aplicando la ecuación de
transmisión de error (104) a la definición de lnK:
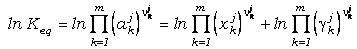 (25b)
(25b)
(ver la
ecuación 25). El cálculo del error en lnK (slnK)
es complicado si las soluciones sólidas no son ideales, particularmente
si los modelos de solución son tan complejos como los presentados más
arriba para el granate y plagioclasa (ecuaciones 91 y 103,
respectivamente). No obstante, el cálculo se simplifica si las
soluciones sólidas son ideales, de forma que
gkj=1.
En este caso el error transmitido en lnK es:
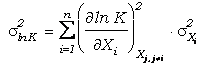 (109)
(109)
donde Xi
son las fracciones molares de los componentes implicados en la reacción
y
sXi son
los errores estándar asignados a cada fracción molar. En esta ecuación
se ha considerado que las Xi no presentan correlación (rXiXj=0),
lo cual significa que no existen dependencias entre las incertidumbres
en las concentraciones de los componentes. Esta simplificación está
justificada siempre que en la expresión de la constante de equilibrio
aparezca un componente por cada fase (e.g., equilibrio GASP). En caso
contrario, existirán correlaciones entre las fracciones molares de los
componentes de una misma fase, ya que éstas se calculan a partir de
normalizaciones atómicas (fórmulas estructurales) en las que la
proporción de cada elemento depende de la del resto de elementos. Así,
en las reacciones de intercambio como el equilibrio GARB existen
correlaciones entre las fracciones molares de almandino y piropo por una
parte (o FeGrt
y MgGrt si se utiliza la expresión de KD) y annita
y flogopita (o FeGrt y MgGrt) por otra. Sin
embargo, para los propósitos de la presente exposición se asumirá que
rXiXj=0.
Aunque la estimación sXi
puede realizarse aplicando de nuevo la ecuación de transmisión de
errores a la definición de las fracciones molares Xi, es
práctica común asumir una incertidumbre relacionable con el error
instrumental (e.g., en torno a 3% relativo).
La Figura 11 muestra las bandas
de error calculadas para el termómetro GARB (calibrado de Ferry y Spear,
1978, con los modelos de solución de Berman,1990, para granate y de
Indares y Martignole, 1985, para biotita) y barómetro GASP (calibrado de
Koziol y Newton, 1988, con los modelos de solución de Berman, 1990, para
granate y de Fuhrman y Lindsley, 1988, para plagioclasa) para la misma
muestra que en la Figura 10. En estos cálculos se han aplicado
las ecuaciones de transmisión de error (108) y (109), considerando una
incertidumbre en P de 1 kbar, de 50 K para en T, de 3% relativo en las
concentraciones atómicas de los elementos y de 20% relativo en los
parámetros de margules de los modelos de solución utilizados. Los
errores en los incrementos de las propiedades termodinámicas de reacción
se han considerado implícitamente sólo para el equilibrio GASP,
asumiendo una incertidumbre de 500 bares para Po (presión
para el equilibrio entre las fases puras a T de interés) y de 0.1%
relativo en el volúmen de las fases puras.
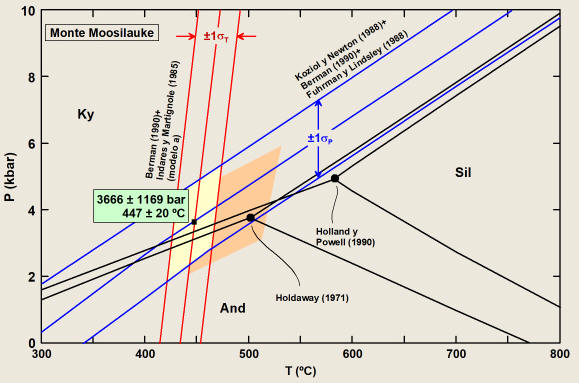
Figura 11.
Bandas de error para el termómetro GARB (calibrado de Ferry y Spear,
1978, con los modelos de solución de Berman,1990, para granate y de
Indares y Martignole, 1985, para biotita) y barómetro GASP
(calibrado de Koziol y Newton, 1988, con los modelos de solución de
Berman, 1990, para granate y de Fuhrman y Lindsley, 1988, para
plagioclasa) para la muestra 90A de Hodges y Spear (1982) del monte
Moosilauke (New Hampshiere, USA). Se indica además la solución P-T
simultánea y las incertidumbres respectivas. El polígono sombreado y
los campos de estabilidad de los polimorfos de Al2SiO5
como en la Figura 10.
Los errores transmitidos en T y P son
cercanos a ±20 ºC y ±1 kbar, respectivamente. Resultados similares se
obtienen considerando otros calibrados/correcciones de los equilibrios.
Puede apreciarse que esta incertidumbre es menor que la resultante de la
aplicación de distintos calibrados/correcciones, particularmente por lo
que respecta a la temperatura.
De hecho, en los cálculos anteriores se
ha considerado un error en los parámetros de margules (asumiendo que no
existen correlaciones entre los mismos) que da cuenta de la imperfección
de los modelos de solución usados, pero no se ha considerado error
alguno asociado a la elección de los calibrados/modelos de
solución. Este error, que da cuenta de la dispersión de soluciones
de T y P, es un error no estadístico
(i.e., no gaussiano), por lo que no puede tratarse mediante la ecuación
de transmisión de errores estadísticos. Esto mismo aplica para el error
resultante de la heterogeneidad composicional de la muestra debida al
mayor o menor grado de equilibrio que presente la asociación de fases.
Su naturaleza no estadística es clara si se tiene en cuenta que este
error da cuenta de la incertidumbre introducida por el pretrólogo al
hacer una interpretación de los datos que le permita la
elección de una composición particular. Estos errores no
estadísticos deben sumarse al error estadístico calculado con la
ecuación de propagación de errores:
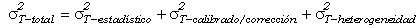 (110)
(110)
Kohn y Spear (1991b) han analizado el
efecto de la elección de distintos modelos de solución para distintos
barómetros y de la heterogeneidad composicional de las fases. Estos
autores concluyen que el error transmitido es fuertemente dependiente
del equilibrio del que se trate y de las condiciones P-T de la muestra.
Por ejemplo, comparando los barómetros GASP y GRAIL (ver Tabla 3), Kohn
y Spear (1991b) concluyen que el primero de ellos es más sensible al
modelo de solución elegido a bajas presiones, mientras que a presiones
elevadas el barómetro GRAIL es más sensible. El rango de incertidumbre
que ofrecen para cuatro barómetros es ±50-1500 bares. La magnitud de la
incertidumbre debida a la heterogeneidad composicional depende del grado
de desequilibrio de la roca. Para muestras que pueden considerarse
cercanas al equilibrio, Kohn y Spear (1991b) indican un rango de
±150-500 bares.
La Figura 12 ilustra
gráficamente los resultados de Kohn y Spear (1991b) para la presión y
temperatura calculadas en una metapelita con el barómetro GASP y el
termómetro GARB. Las elipses representan errores estadísticos y los
paralelogramos representan errores no estadísticos. La elipse pequeña es
el error transmitido debido a la precisión en el análisis de las fases
(±150 bares). La elipse alargada representa el error transmitido por los
errores en los incrementos de las propiedades termodinámicas de las
reacciones, que en este caso son los errores en las calibraciones
experimentales (±1700 bares). El paralelogramo pequeño oscuro representa
el error no estadístico resultante de la heterogeneidad composicional de
la muestra (±500 bares), y el paralelogramo más grande representa el
error no estadístico resultante de la elección de modelos de solución
(±900 bares). La consideración de todas las fuentes de error resulta en
una incertidumbre de ±3100 bares, lo cual es un error considerable si se
tiene en cuenta que corresponde a ±11 km.

Figura 12.
Diagrama P-T con indicación de las incertidumbres calculadas en la
aplicación del barómetro GASP y termómetro GARB. Las elipses blancas
pequeña y grande representan los errores estadísticos propagados
debidos a la precisión analítica y a los errores en las
calibraciones de los equilibrios (i.e., incertidumbre en las
propiedades termodinámicas de los componentes puros),
respectivamente. Los paralelogramos oscuros pequeño y grande
representan las incertidumbres no estadísticas debidas a la elección
de un conjunto de composiciones (ie., heterogeneidad composicional)
y de los modelos de solución, respectivamente. La región sombreada
más grande representa la combinación de todos los errores. Figura
tomada de Kohn y Spear (1991b).
Notas
Esto
se debe a que algunas variables se extraen a partir de otras. Por ejemplo,
la estimación de DHro(1,298)
y
DSro(1,298)
a partir de datos experimentales se realiza previo conocimiento de
DVro(1,298).
[Back] [Home] [Up] [Next]
Última
modificación:
domingo, 05 de octubre de 2025 15:27 +0200 |