
![]() COCHLEAR
IMPLANT
SIMULATION
version 2.0
COCHLEAR
IMPLANT
SIMULATION
version 2.0

| Page principale |
|
Le programme « Cochlear Implant Simulation » a été développé en partant d’un modèle qui représente les principales étapes du processus par lequel un patient muni d’un implant cochléaire perçoit le son. Dans ce modèle on considère des aspects techniques ainsi que physiologiques qui conditionnent la perception du son. Le processus est partagé en deux blocs principaux : un bloc d’analyse et un bloc de synthèse.
Le bloc d’analyse représente le processus que suit le signal audio depuis son acquisition par le microphone jusqu’à sa transformation en impulsions électriques, fournies par les différentes électrodes de l’implant, et qui donnent lieu aux potentiels d’action sur le nerf auditif.
La première partie du bloc considère exclusivement le traitement du signal fait par le système d’implant cochléaire, et permet de représenter la perte d’information associée à la configuration de l’implant et la stratégie de codage. La deuxième partie du bloc d’analyse représente l’interaction entre le faisceau d’électrodes et les terminaisons nerveuses et décrit comment la configuration de l’activité des électrodes de l’implant est transformée en configuration d’activité sur le nerf auditif.
Le bloc de synthèse fournit un signal audio à partir de la configuration de l’activité du nerf auditif obtenue dans le bloc d’analyse. Le signal audio est synthétisé à partir de la configuration de l’activité de chaque bande de fréquence (associée à chaque région de la cochlée). De cette façon, l’information perdue au cours du processus d’analyse donne lieu à une perte de qualité dans le signal synthétisé. La figure 1 représente le diagramme des blocs considéré pour la simulation.
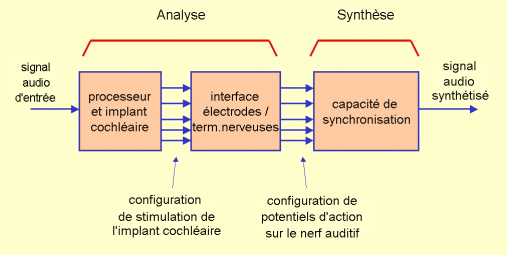
Figure 1: Diagramme des blocs du programme ``Cochlear Implant Simulation".
Ce modèle permet de considérer les principaux aspects qui influent sur la perception fournie par l’implant tels que la stratégie de codage, la conception de la banque de filtres, la fréquence de stimulation, le nombre de canaux, les dimensions de l’implant cochléaire, l’emplacement du faisceau d’électrodes, l’interaction entre les électrodes de l’implant et les terminaisons nerveuses, etc. Les signaux synthétisés compte tenu de ce modèle représente la perte d’information propre de la stimulation par l’implant et permettent, de cette façon, aux individus normo-entendents d’écouter le son tel qu’il serait perçu par un patient porteur d’implant cochléaire.La figure 2 montre le diagramme de blocs d’un système d’implant cochléaire conventionnel. Le signal est acquis par le microphone du processeur, puis amplifié et passé par une banque de filtres qui le sépare en différentes bandes de fréquence. La sortie de chaque filtre passe par un détecteur d’enveloppe. De cette façon, pour chaque canal, on estime l’énergie du signal sur chaque bande de fréquence et à chaque instant. Le bloc d’adaptation de rang dynamique sert à transformer le rang dynamique acoustique de chaque canal, en rang dynamique électrique exigé par chaque électrode du patient. Cette transformation du rang dynamique est spécifique au patient et différente pour chacune des électrodes. Finalement, selon la fréquence de stimulation, le processeur génère des impulsions de stimulation qui représentent le niveau de courant qu’on doit fournir sur chaque électrode à chaque instant. Dans les stratégies de codage pulsées (comme les stratégies CIS ou n-of-m) les impulsions de stimulation sont générées de façon à ce que, à chaque instant, il y ait uniquement une électrode active dans le but d’éviter le phénomène nommé « l’addition de champs ». Une fois la configuration de stimulation établie dans le processeur, celle-ci est alors transmise à l’implant cochléaire puis les impulsions de courant sont générées par les électrodes de l’implant.
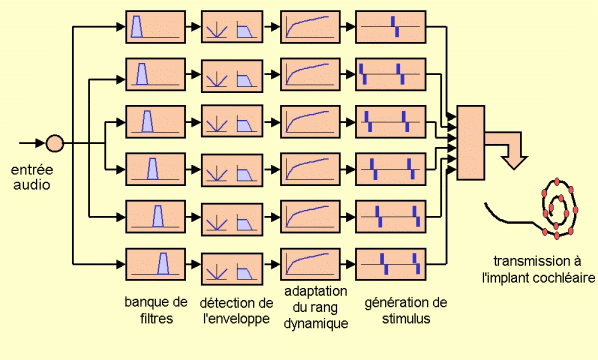
Figure 2: Diagramme de blocs d'un système d'implant cochléaire.
Le programme « Cochlear Implant Simulation » traite le son en reproduisant l’analyse du signal réalisée par le processeur de l’implant cochléaire, en accord avec l’ensemble des paramètres de simulation établis. Cette analyse fournit la configuration d’activité sur les électrodes de l’implant cochléaire qui serait obtenue à la présentation du signal audio au microphone.
A partir de la configuration d’activité sur les électrodes, et en accord avec le modèle d’interaction entre les électrodes et les terminaisons nerveuses, on détermine la configuration de l’activité neurale des groupes de terminaisons nerveuses associés à chaque portion cochléaire. Finalement, on synthétise le signal audio en partant de cette configuration d’activité neuronale, tout en tenant compte de la capacité de synchronisation de l’activité neuronale et des fréquences caractéristiques des portions cochléaires stimulées.
La fréquence de stimulation représente le nombre d’impulsions par seconde qui sont présentés sur chacune des électrodes de l’implant cochléaire. Ce paramètre limite la résolution temporelle de l’implant cochléaire, c’est-à-dire, la capacité de percevoir des changements rapides des caractéristiques du signal audio. Plus la fréquence de stimulation est petite, plus la qualité du son perçu est mauvaise.
La résolution temporelle avec laquelle le patient perçoit le son est limitée, non seulement par la fréquence de stimulation, mais par la période réfractaire des neurones du nerf auditif. Le temps nécessaire pour la repolarisation des neurones après une décharge est d’environ 2 ms. C’est pour cela qu’il est préférable de régler la fréquence de stimulation au-dessus de 1000 impulsions par seconde.
Dans le programme « Cochlear Implant Simulation », la fréquence de stimulation est représentée en sous-échantillonnant les enveloppes à la fréquence de stimulation. Il faut tenir compte de l’existence de stratégies de stimulation où l’on utilise une fréquence d’actualisation de l’enveloppe inférieure à la fréquence de stimulation. Dans ce cas, la valeur assignée au paramètre « fréquence de stimulation » correspond à la fréquence (taux) d’actualisation de l’enveloppe, puisque ce paramètre représente la perte de résolution temporelle.
Il faut prendre en compte que, pour des fréquences de stimulation excessivement basses (en dessous de 800 ou 700 pps), en plus de la perte de résolution temporelle, se produit un effet de synchronisation de l’activité neuronale avec les impulsions de stimulation, ce qui réduit encore plus la qualité de perception chez le patient implanté. Cet effet n’a pas été modelé dans le programme « Cochlear Implant Simulation » ainsi, dans le cas de fréquences de stimulation très basses, la qualité du signal perçu dans la situation réelle est plus mauvaise que celle fournie par la simulation.
La banque de filtres utilisée pour l’analyse est composée de filtres équidistants sur une échelle logarithmique de fréquence dans le rang défini par fMin et fMax. Les bandes passantes des filtres sont égales sur l’échelle logarithmique de fréquence, de façon à ce que les bandes correspondantes à des fréquences plus basses soient plus étroites et que celles correspondantes à des fréquences plus hautes soient plus larges.
Chaque canal de l’implant cochléaire possède un filtre passe-bande. Le nombre de canaux est déterminé par le paramètre « n-insérés-ic ». Plus le nombre de canaux est grand, plus la résolution spectrale tonotopique est grande. Dans le cas où l’option « Hilber+FIR » est sélectionné, les filtres sont conçus comme des filtres à réponse impulsionnelle finie (FIR) à 100 coefficients. Dans le cas où l’option « Rect-LP+IIR » est sélectionné, on utilise des filtres à réponse impulsionnelle infinie (IIR) de type Butterworth de 6e ordre. Les filtres FIR ont l’inconvénient d’avoir besoin d’une plus grande quantité de calculs. D’autre part, les filtres IIR ont les inconvénients de causer une distorsion de phase et de pouvoir donner une réponse instable, particulièrement dans le cas de petites bandes passantes.
La détection de l’enveloppe est réalisée grâce à un redressement et un filtrage passe-bande (option « Rect-LP+IIR ») ou bien grâce à la transformée de Hilbert (option « Hilbert+FIR »). Cette dernière option fournit une enveloppe qui représente de façon optimale l’évolution temporelle de l’énergie dans la bande de fréquence du filtre, mais elle a l’inconvénient de demander l’utilisation de deux filtres FIR en quadrature de phase, avec l’augmentation du nombre de calculs correspondants.
Le paramètre « n-of-m » permet de sélectionner des stratégies CIS (lorsque n est égal à m, c’est-à-dire, au nombre de canaux insérés) ou des stratégies n-of-m (lorsque n est inférieur à m).
Les stratégies n-of-m fonctionnent en activant, dans chaque cycle de traitement, uniquement les n canaux qui présentent le plus d’énergie parmi les m disponibles. Le but des stratégies n-of-m est de permettre un accroissement de la fréquence de stimulation grâce à la réduction du nombre de canaux activés dans chaque cycle, ce qui réduit la durée totale du cycle de traitement. Cet accroissement de la fréquence de stimulation est fait au dépend d’une réduction de la qualité, puisque l’information correspondante aux canaux non sélectionnés est perdue.
Pour simuler l’effet des stratégies n-of-m, dans chaque cycle de traitement, on compare les enveloppes correspondantes aux différents canaux puis on sélectionne les n les plus énergétiques et on annule les enveloppes du reste des canaux. De cette façon, l’information correspondante aux canaux non sélectionnés est éliminée du signal synthétisé.
L’interaction entre les canaux est modelée par l’interface électrodes – terminaisons nerveuses. Dans des travaux préalables, on a estimé la distribution de densité de courant dans un système électrique semblable à la cochlée stimulée par un implant cochléaire. On a trouvé que le courant émis sur une électrode se disperse sur une surface relativement étendue, dans le cas de stimulation monopolaire comme de stimulation bipolaire.
Quand on stimule sur une électrode, il serait souhaitable que seulement les fibres nerveuses les plus proches de l’électrode soient activées. Cependant, les pulses présentés sur une électrode activent ces fibres mais aussi d’autres plus éloignées. De façon analogue, un groupe de fibres va être activé principalement par l’électrode la plus proche, mais il va aussi s’activer lorsqu’il y aura des stimulus sur des électrodes plus éloignées. Ce phénomène peut être modelé grâce à une matrice de mélange entre les canaux de l’implant et les « canaux du nerf auditif », en définissant chacun de ces canaux comme le groupe de neurones voisins à une électrode. De cette façon, les différents canaux de l’implant contribuent à chaque « canal du nerf auditif », et la contribution dépend de la distance qui sépare chaque électrode de la partie cochléaire considérée. Dans ce modèle, on a supposé que la contribution diminue de façon exponentielle avec la distance, et on définit le coefficient d’interaction comme la constante de cette baisse exponentielle. Les études sur la distribution du champ de courant dans la cochlée suggèrent qu’une valeur appropriée pour cette constante est d’environ 2 ou 3 mm.
Pour déterminer la matrice de mélange qui donne lieu à l’interaction entre les canaux, on tient compte de la d entre les différentes électrodes de l’implant. Pour cela, on considère les dimensions de l’implant et le nombre d’électrodes qu’il possède. Plus les électrodes sont proches entre elles ou bien plus le coefficient d’interaction est grand, plus l’interaction entre les canaux est grande, ce qui a pour conséquence une perte de résolution spectrale tonotopique. Dans ce cas, la résolution spectrale fournie par l’implant ne va pas être limitée par le nombre d’électrodes mais par l’interaction entre les canaux. On peut apprécier que, pour des petites valeurs du coefficient d’interaction, la qualité du signal synthétisé augmente suivant le nombre d’électrodes considérées dans la simulation. Cependant, pour de plus grandes valeurs du coefficient d’interaction, la résolution spectrale ne s’améliore plus si la distance entre les électrodes adjacentes est inférieure au coefficient d’interaction.
Le bloc de synthèse du signal correspond au diagramme montré sur la figure 3. La synthèse part de la configuration d’activité après avoir modelé l’interaction entre les canaux. L’enveloppe de chaque canal représente l’énergie qu’il y a pour chacune des bandes de fréquence et à chaque instant. C’est pour cella que l’on utilise un signal d’excitation (d’abord, avec une distribution d’énergie uniforme sur la fréquence et sur le temps) pour synthétiser le signal audio. Cette excitation est filtrée avec une banque de filtres puis le signal filtré est multiplié par l’enveloppe. Après ces opérations, la sortie de chaque canal est un signal limité dans la bande définie par le canal dont l’énergie évolue dans le temps suivant l’enveloppe considérée. Finalement, on additionne les contributions provenant des différents canaux en obtenant un signal audio qui comprend les contributions dans tout le rang spectral traité.
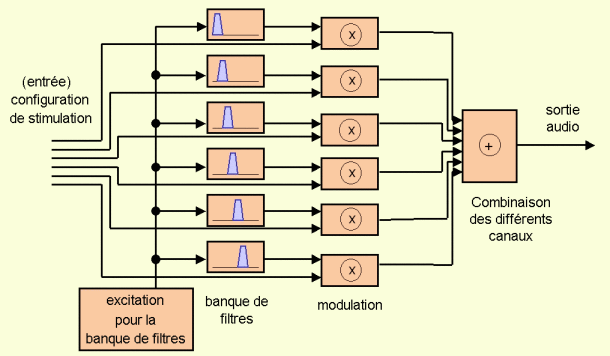
Figure 3: Diagramme du bloc de synthèse du signal du programme ``Cochlear Implant Simulation".
Le signal d’excitation considéré peut être un bruit blanc gaussien puisque cette excitation présente un spectre plat et une distribution d’énergie uniforme dans le temps. Cependant, les signaux synthétisés en utilisant un bruit blanc présentent une très mauvaise qualité due au fait que la phase du signal synthétisé soit aléatoire, car l’excitation utilisée pour chaque canal est aussi aléatoire. Le résultat est un signal audio qui perd la structure temporelle et, en particulier, il perd le ton fondamental qui ne peut pas être résolu dans le domaine temporel. Plusieurs expériences ont mis en évidence que la plupart des patients perçoivent avec une meilleure qualité par rapport à celle obtenue en synthétisant de cette façon. Pour cela, on propose une méthode alternative de synthèse. Celle-ci consiste à utiliser comme signal d’excitation un ensemble de pulses. Les pulses sont situés dans les instants où l’enveloppe a un maximum local. Un pulse isolé ou un ensemble de pulses ont un spectre plat. Pour éviter que l’énergie du signal synthétisé soit conditionnée par les pulses (elle doit dépendre des enveloppes mais non des excitations du bloc de synthèse) le signal d’excitation est normalisé pour qu’il ait une distribution d’énergie la plus uniforme possible dans le temps. Dans cette méthode de synthèse, l’excitation présentée pour chaque bande est indépendante du reste des bandes et elle est calculée à partir des maximums locaux des enveloppes considérées dans la bande correspondante.
L’utilisation d’une excitation de type bruit blanc gaussien représente comment perçoit un patient implanté qui n’a pas une bonne résolution temporelle à cause d’une lésion du nerf auditif. Cette situation fait que l’activité neurale ne soit pas synchronisée avec le stimulus auditif et que le ton fondamental ne reste pas représenté dans la configuration de l’activité neurale. Cette façon de percevoir le son se présente chez les patients avec pertes auditives plus prolongées ou lorsque le taux de survie neuronale est plus bas, c’est-à-dire, quand les lésions cochléaires sont plus étendues.
L’utilisation d’une excitation de type train de pulses représente comment on perçoit le son chez un patient implanté avec une bonne capacité de synchronisation de l’activité neurale. Dans ce cas, la configuration d’activité du nerf auditif peut suivre l’évolution de l’enveloppe, produisant la plupart des décharges aux instants où l’enveloppe a un maximum d’énergie. De cette façon, le ton fondamental peut être perçu à partir de la configuration temporelle de l’activité du nerf auditif.
Dans un cas réel, il est à prévoir que le patient aura une perception avec une qualité intermédiaire entre les deux situations, plus proche de la situation de « mauvaise synchronisation » quand les lésions cochléaires sont plus importantes, et plus proche à une « bonne synchronisation » quand le nerf auditif se trouve dans un meilleur état. Afin de modeler cet effet, le logiciel « Cochlear Implant Simulation » calcule les deux signaux d’excitation (bruit blanc gaussien et train de pulses) et les combine en fonction du paramètre de synchronisation.
La banque de filtres utilisée pour la synthèse est constitué de filtres passe-bande de type FIR, dans le but de ne pas introduire de distorsions de phase inutiles dans le traitement de synthèse. Si l’option « Déplacement de Fréquences » n’est pas sélectionnée, les fréquences centrales et les fréquences de coupure des filtres concordent avec celles de la banque de filtres utilisés pour le bloc d’analyse. Si cette option est sélectionnée, les fréquences et les bandes passantes des filtres de synthèse sont déterminées en tenant compte de la position de chaque électrode et de la fréquence caractéristique correspondante à cette position selon la théorie tonotopique. Pour cela, on tient compte aussi bien des dimensions du faisceau d’électrodes que du nombre d’électrodes et de la profondeur d’insertion du faisceau.
Pour simuler la perception dans le cas de Stimulation Electro-Acoustique (EAS ou Electro-Acoustic Stimulation en anglais) on sépare le spectre en une partie basse (correspondante à la stimulation acoustique) et une partie haute (correspondante à la stimulation électrique). Pour séparer les deux parties, on tient compte du paramètre « fréquence de coupure ». La partie de stimulation acoustique est obtenue en filtrant passe-bas le signal original avec un filtre conçu avec cette fréquence de coupure. La partie de stimulation électrique est obtenue en traitant le signal en accord avec la configuration de l’implant cochléaire et en utilisant comme rang de fréquences celui déterminé par la fréquence de coupure et par fMax. Le signal synthétisé est obtenu en additionnant la partie de stimulation acoustique et la partie de stimulation électrique.
Pour valider la méthode de simulation mise en œuvre dans le programme « Cochlear Implant Simulation », on a effectué des tests en présentant des phrases à plusieurs patients porteurs d’implant cochléaire. Dans ces tests, on a présenté différentes phrases, synthétisées mais aussi originales. On demandait au patient d’évaluer la qualité dont les phrases synthétisées et originales étaient perçues.
Pour réaliser la validation, l’hypothèse de départ est que la simulation comme le système d’implant cochléaire donnent lieu à une perte de qualité de l’audition. Dans les tests, le patient implanté va percevoir une phrase traitée par le programme de simulation puis celle-ci traitée par le propre système d’implant cochléaire dont il est porteur (dans le cas de phrases synthétisées), ou bien une phrase uniquement traitée par le système d’implant cochléaire (dans le cas de la phrase originale).
Quand la simulation est réalisée avec une configuration qui fournit une qualité meilleure que les paramètres du système d’implant cochléaire, la qualité de la phrase synthétisée ne va pas être conditionnée par les paramètres de simulation. Dans ce cas, en accord avec l’hypothèse de départ, le patient devrait indiquer que la qualité de la phrase synthétisée est semblable à celle de la phrase originale. Quand on réalise la simulation avec une configuration qui fournit une qualité plus mauvaise que les paramètres du système d’implant cochléaire, la qualité de la phrase synthétisée sera conditionnée par les paramètres de simulation. Dans ce cas, le patient devrait indiquer que la phrase synthétisée a une plus mauvaise qualité que l’originale.
De cette façon, on fixe tous les paramètres de simulation aux valeurs détenues par le système d’implant cochléaire du patient, sauf un parmi eux, que l’on fait varier depuis une bonne valeur (laquelle fournit une meilleure qualité) à une autre plus mauvaise (laquelle fournit une qualité pire) et puis on représente graphiquement la qualité par rapport à ce paramètre : la qualité tend à être bonne (semblable pour la phrase originale et synthétisée) et vers les mauvaises valeurs présente un chute (la phrase synthétisée est perçue clairement plus mauvaise que la phrase originale). Cette courbe devrait présenter un coude juste au moment où la valeur du paramètre de simulation concorde avec la valeur du paramètre de son système d’implant cochléaire. Si cet effet est vérifié, on peut conclure que la simulation modèle de façon adéquate l’effet de ce paramètre sur la qualité de l’audition.
On a réalisé plusieurs tests de validation sur 7 patients porteurs d’implant cochléaire. Tous ont été implantés au service d’ORL de l’Hôpital La Paz de Madrid avec un dispositif Combi40+ fabriqué par MED-EL. Les tests de validation ont été centrés sur 3 paramètres de simulation : la fréquence de stimulation, le nombre de canaux et le coefficient d’interaction entre les canaux. Pour chacun d’entre eux, on a synthétisé des phrases avec différentes valeurs du paramètre à étudier et on a présenté au patient aussi bien les phrases originales que celles synthétisées, et on lui a demandé d’évaluer la qualité dont il perçoit chacune des phrases dans une échelle entre 0 (très mauvaise qualité) et 10 (qualité optimale).
Pour l’analyse de résultats, la note indiquant la qualité des phrases a été normalisée en la divisant par la note attribuée à la phrase originale correspondante. De cette façon, si une phrase synthétisée a une note de 1, on doit interpréter que le patient la perçoit avec la même qualité que la phrase originale. Pour chaque paramètre étudié, on a représenté la note normalisée par rapport au paramètre considéré. On a réalisé un ajustement polynomial (de 3e ordre) sur un critère d’erreur quadratique minimale sur ces données, obtenant ainsi la fonction qui s’ajuste le mieux aux données et les intervalles de confiance de 95 % correspondants.
Dans la figure 4, on montre les valeurs des notes de qualité normalisée par rapport à la fréquence de stimulation considérée dans la simulation. On montre aussi l’ajustement de ces données. Chaque point du graphique représente l’évaluation par un patient d’une phrase synthétisée. On montre l’ajustement polynomial sur un critère de minimum d’erreur quadratique et l’intervalle de confiance de 95 % correspondant. On peut observer que, pour de très hautes fréquences de stimulation, les patients n’aperçoivent pas de perte de qualité dans les phrases synthétisées et, à mesure que la fréquence est plus petite, la qualité diminue, obtenant ainsi de très basses notes pour des fréquences au-dessous de 700 pps. On observe l’effet de coude dans le graphique correspondant à chaque patient. En plus, on s’aperçoit que la fréquence où se trouve le coude est différente pour chaque patient, celle-ci étant plus grande lorsque la fréquence utilisée par le processeur est plus grande. Ce résultat valide le procédé de simulation par rapport à la fréquence de stimulation.
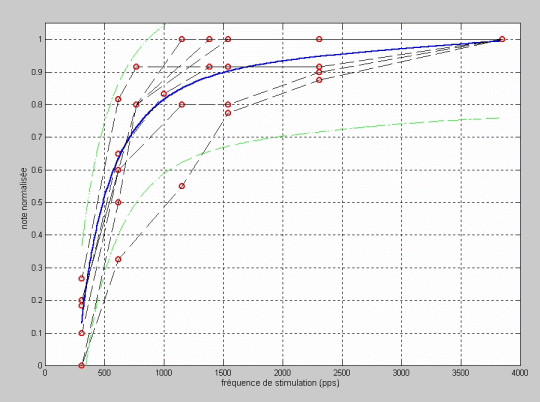
Figure 4: Ajustement de la note de qualité normalisée par rapport à la fréquence de stimulation.
Pour vérifier l’influence de la fréquence de stimulation de la simulation par rapport à celle programmée dans le processeur du patient, on a réalisé un ajustement, en utilisant comme variable indépendante la fréquence de stimulation utilisée pour la simulation et la fréquence utilisée dans le processeur. Les résultats de cet ajustement sont montrés dans la figure 5. Dans ce cas, on aperçoit que le coude est placé autour d’une valeur de fréquence de stimulation normalisée proche à l’unité, c’est-à-dire, quand la fréquence de stimulation de la simulation se rapproche de celle programmée dans l’implant du patient.
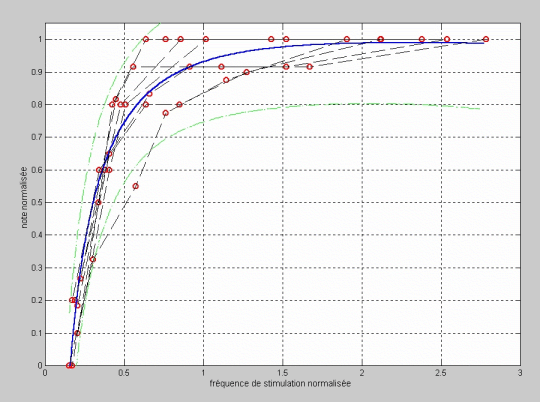
Figure 5: Ajustement de la note de qualité normalisée par rapport à la fréquence de stimulation normalisée.
La figure 6 montre l’ajustement entre la note de qualité normalisée et le nombre de canaux utilisés dans la simulation. Les patients disposaient d’ajustements du processeur avec un nombre d’électrodes actives situé entre 9 électrodes et 12 électrodes (2 patients avec 9 électrodes actives, 1 avec 10 électrodes, 1 avec 11 électrodes et 3 avec 12 électrodes).
Dans ces courbes graphiques, on observe l’effet de coude où la qualité ressemble à celle de la phrase originale pour un grand nombre de canaux pour la simulation, et on observe une dégradation rapide quand le nombre de canaux utilisé pour la simulation est inférieur à 8. Il est intéressant que le coude ne soit pas autour du nombre de canaux qu’utilise le patient mais vers 8 canaux. Ceci met en évidence que la résolution spectrale tonotopique que ces patients jouissent n’est pas conditionnée par le nombre d’électrodes mais par un autre phénomène. La résolution spectrale tonotopique dont ils perçoivent le son est celle équivalente à environ 8 canaux, malgré le fait de disposer d’un plus grand nombre de canaux actifs dans leurs implants respectifs. La cause probable de cette limitation de la résolution spectrale tonotopique est l’interaction entre les canaux.
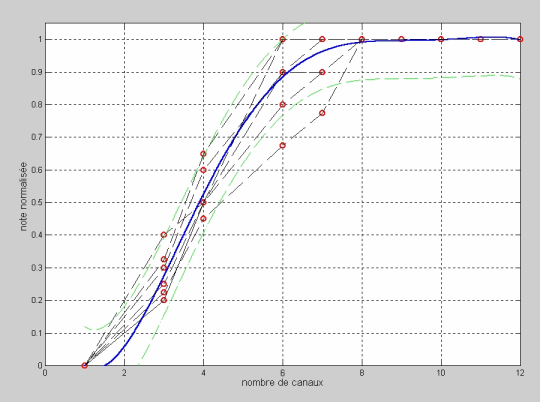
Figure 6: Ajustement de la note de qualité normalisée par rapport au nombre de canaux.
Pour évaluer l’effet d’interaction entre les canaux, on a réalisé des tests en modifiant dans la simulation le coefficient d’interaction entre les canaux. Les résultats sont montrés dans la figure 7. On observe que, quand on synthétise le signal avec un petit coefficient d’interaction, la qualité de la phrase synthétisée est semblable à celle de la phrase originale mais, à mesure que ce coefficient d’interaction augmente, la qualité se dégrade de façon importante. Le coude dans ces courbes est placé vers 1 ou 2 mm, ce qu’on peut interpréter comme suit : l’interaction entre les électrodes et les terminaisons nerveuses peut être modelée par le coefficient d’interaction entre les canaux en donnant à ce coefficient une valeur proche à 1 ou 2 mm. Cette valeur est consistante avec les observations et les études théoriques préalables concernant la distribution de la densité de courant dans le système électrique implant cochléaire – cochlée.
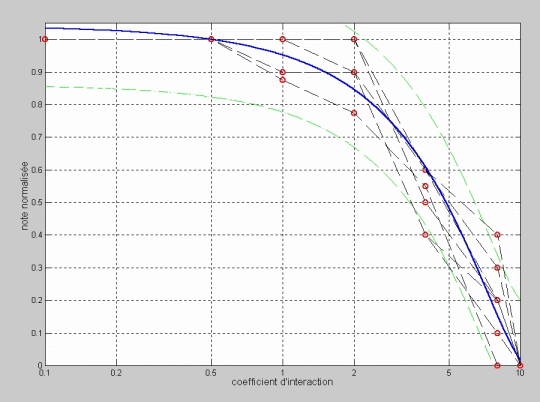
Figure 7: Ajustement de la note de qualité normalisée par rapport au coefficient d'interaction.
Les auteurs remercient l’équipe d’ORL de l’Hôpital La Paz de Madrid de la collaboration rendue et remercient aussi les patients qui ont participé aux tests de validation de leur participation.