Prácticas: Control de calidad
El análisis de calidad de los análisis químicos con WDS o EDS pasa por
los siguientes pasos.
-
El análisis se suministra
% peso de elementos o de óxidos.
-
El análisis de O es más impreciso dado que es
ligero. Suele no analizarse,
dándose entonces por estequiometría (el total de carga positiva
deben ser igual a la carga debida al oxígeno una vez descontadas las
cargas de otros aniones, en su caso) ya sea como O si el análisis se
suministra en elementos, ya sea como ligado a los elementos en
óxidos. Esto último es lo más habitual.
-
Vaya a página Cuantificación de la señal >> 5c.- Criterios de exactitud (calidad).
-
Valorar la cercanía a 100% de la suma de las concentraciones elementales
u óxidos en peso (con O estimado o medido). Esto es válido solo para
sustancias que no tengan H. Si el total
en % en peso no se aproxima a 100 en este tipo de sustancias:
-
Defectos en el calibrado.
-
Defectos del
pulido, análisis en fracturas o en superficie irregular.
-
Cubierta de
grafito defectuosa.
-
Cubierta de
grafito con grosor sustancialmente diferente al de los
patrones (más fino o más grueso).
-
Daños en la
muestra.
-
Falta
algún elemento importante por analizar. Por ejemplo, Zn en
estaurolita o Ba en feldespato-K o moscovita. En silicatos,
normalmente se analizan Si, Ti, Al, Fe, Mn, Mg, Ca, Na y K. En
rocas máficas/ultramáficas, se suelen añadir Cr, Ni ±Co. En
algunos casos, se suele añadir Zn, Ba, F, Cl, P. Para valorar esto
debe realizarse un espectro
de longitud de onda (mejor) o de energía.
-
Problemas experimentales (e.g., altibajos en
la corriente de sonda).
-
Estado de oxidación variable en algún
elemento. Los más comunes son Fe y Mn, y en mucha menor medida a
Ti. Por ejemplo, si se expresa Fe como FeOtotal en
una fase rica en Fe3+, como
hematites
(o hematita): 100% Fe2O3 = 89.98% FeO). En el caso de
andradita:
|
Andradita: Ca3Fe3+2(SiO4)3 |
|
|
SiO2 |
35.47 |
SiO2 |
35.47 |
|
Fe2O3 |
31.42 |
FeO |
28.28 |
|
CaO |
33.11 |
CaO |
33.11 |
|
Total |
100.00 |
Total |
96.85 |
-
El H no se puede
analizar. Por ello, el análisis de los minerales o sustancias (e.g.,
vidrio volcánico, cerámica) con H no sumará 100% en peso. Las
cantidades de H o H2O % en peso se pueden estimar por estequiometría
asumiendo unas cantidades moleculares de (OH)- y/o de H2O
dadas. Por ejemplo,
moscovita KAl2(Si3Al)O10(OH1.8,F0.2),
asumiendo los valores dados de OH (= 2-F) y calculando el oxígeno
teórico:
|
Si |
21.13 |
SiO2 |
45.21 |
|
Al |
20.30 |
Al2O3 |
38.36 |
|
K |
9.81 |
K2O |
11.81 |
|
F |
0.95 |
F |
0.95 |
|
H |
0.46 |
H2O |
4.07 |
|
O |
47.35 |
|
|
|
|
|
Suma |
100.40 |
|
Total |
100.00 |
Total |
100.00 |
lawsonita: CaAl2Si2O7(OH)2·H2O),
asumiendo los valores dados de OH y H2O y
calculando el oxígeno teórico:
|
Si |
17.88 |
SiO2 |
38.24 |
|
Al |
17.17 |
Al2O3 |
32.45 |
|
Ca |
12.75 |
CoO |
FALSO |
|
H |
1.28 |
H2O |
11.47 |
|
O |
50.91 |
|
|
|
Total |
100.00 |
Total |
100.00 |
-
Algunos elementos ligeros ((Li, Be, B, C, N, O...) necesitan
cristales específicos con
espaciado muy grande y pueden analizarse mal. Generalmente no se
analizan (el O se calcula por estequiometría). El C en los
carbonatos se estima por estequiometría (igual que O en silicatos y
óxidos).
-
Si se analizan los aniones (típicamente, O, ±Cl,
±F; S en sulfuros) y cationes: Valorar el balance de carga tras
calcular los moles de aniones y cationes (= % peso/peso atómico)
teniendo en cuenta el hidrógeno teórico.
-
Valorar la estequiometría de las fórmulas minerales.
· Los porcentajes en peso de elementos u óxidos se utilizan
habitualmente para el cálculo de las fórmulas estequiométicas de un mineral o material. Este cálculo estequiométrico generalmente se basa en una cantidad
fija de oxígenos, azufre, cationes o metales, según la muestra
analizada.
·
Materiales para el
cálculo de fórmulas minerales se pueden encontrar en el módulo
Enseñando Equilibrios de Fase; estos
materiales incluyen hojas de
cálculo y recursos en línea relacionados para calcular las fórmulas
estructurales de la mayoría de los minerales formadores de rocas
· Vea
también: Chemical Composition y Mineral Formulae from Chemical Analyses de A.
Garcia-Casco.
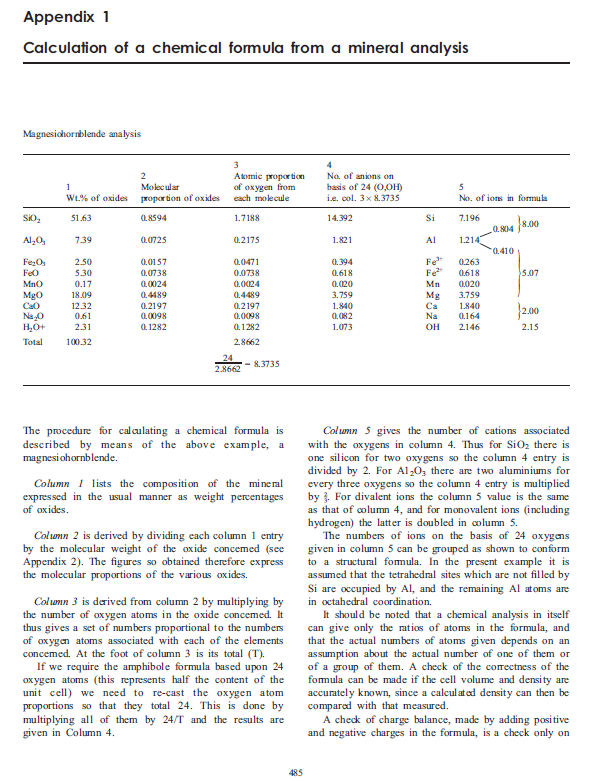
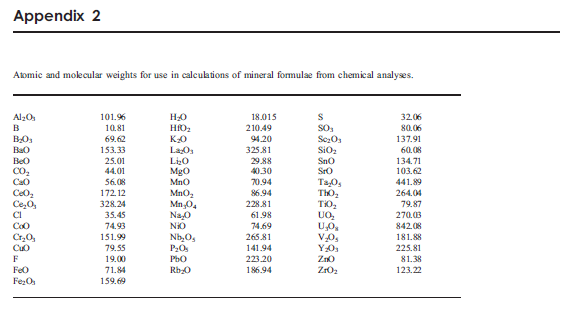
· Vea también: Apéndices 1 y 2 de
W. A. Deer, FRS; R. A. Howie; J. Zussman
(2013). An Introduction to the Rock-Forming Minerals.
Mineralogical Society of Great Britain and Ireland. 498 pp.
DOI: 10.1180/DHZ (en estos ejemplos se tiene un conocimiento de la
concentración de H2O que por WDS/EDS no se puede
obtener).


· Vea Webmineral o
Mindat para fórmulas minerales.
-
Problema de análisis "mezcla"
de fases por fluorescencia
secundaria. Visualizar las proporciones atómicas o moleculares
de los minerales en diagramas binarios, ternarios y cuaternarios.
Ejemplo 1.
1993. GARCÍA CASCO, A., SANCHEZ NAVAS, A., TORRES ROLDAN, R.L.
Disequilibrium decomposition and breakdown of muscovite in high P-T
gneisses, Betic Alpine Belt (Southern Spain). American
Mineralogist 78, 158-177.



Ejemplo 2.
2013. GARCIA-CASCO, A., KNIPPENBERG, S.,
RODRÍGUEZ RAMOS, R., HARLOW, G.E, HOFMAN, C., POMO, J.C.,
BLANCO-QUINTERO, I.F. Pre-Columbian jadeitite artifacts from the
Golden Rock Site, St. Eustatius, Lesser Antilles, with special
reference to jadeitite artifacts from Elliot’s, Antigua:
Implications for potential source regions and long-distance exchange
networks in the Greater Caribbean. Journal of Archaeological
Science, 40, 3153–3169. DOI 10.1016/j.jas.2013.03.025.

Fig. 7. Binary
diagrams showing the composition of analyzed clinopyroxenes
expressed in terms of cations per formula unit (6 oxygens), with
indication of significant end-members and exchange vectors.

Fig. 8. Composition
of jadeite and omphacite plotted in the ternary jadeite-q-aegirine
diagram with the clinopyroxene classification scheme of Morimoto
et al. (1988;
names in italics). Also shown are the phase relations of
clinopyroxene (denoted by space groups C2/c and P/2n) calculated by Green
et al. (2007) at
500 °C in the system jadeite-diopside-aegirine. Note that jadeite
and omphacite with higher q component plot within the omphacite-jadeite
and omphacite-diposide solvus (forbidden regions) as a likely
consequence of the lack of consideration of hedenbergite in
the calculated phase relations and/or different temperature of
formation. Solid lines indicate varying aegirine/(q + aegirine)
ratios.

Fig. 5. ACFN
“deluxe” diagrams for the analyzed minerals of the studied artifacts
calculated with CSpace (Torres-Roldán
et al., 2000).
The minerals are projected from the phases and exchange vectors
indicated in A. Representative end-members of the solid solutions
are indicated (lower case font).
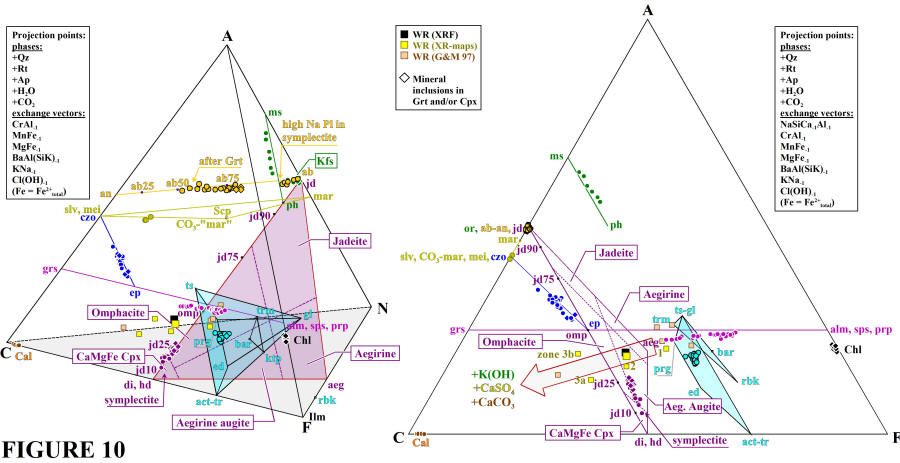
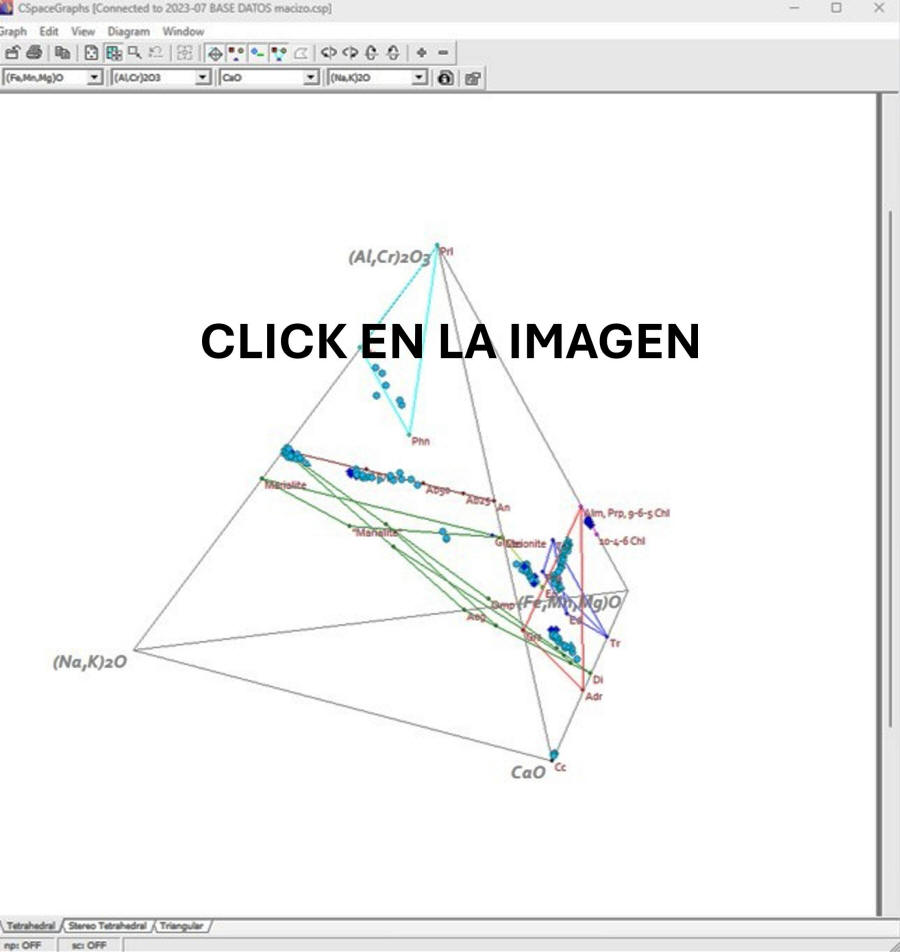
Diagrama cuaternario ACFN generado con
CSpace.
Para ver el video, click en la imagen. Se recomienda visualizarlo en
bucle y a escasa velocidad.
|