![\begin{figure}\includegraphics[bb= 100 370 500 705]{fig2.ps}
\end{figure}](Timg81.gif) |
Consideramos el radon separadamente por dos razones: puede producir dosis con grandes variaciones en localizaciones concretas y además no es evidente si esta fuente pertenece a la categorıa de natural o artificial. El origen del radon es, por supuesto, natural, puesto que es producido por los isótopos primigenios en la corteza terrestre. No obstante, la severidad del problema del radon depende en gran medida de la naturaleza y localización del edificio en donde se esté habitualmente. La magnitud del problema del radon se ha incrementado desde la aparición de edificaciones muy eficientes en materia de aislamiento. Tales edificios conservan muy bien el calor, pero también otros materiales que se liberan en su interior. Esto incluye al gas radiactivo radon y a los productos de su desintegración.
El radon es uno de los productos de la desintegración del
![]() U, como se ve en la figura 2. El radon es un emisor
U, como se ve en la figura 2. El radon es un emisor
![]() y
y ![]() con semivida relativamente corta (3.8 d)
y la caracterıstica que lo hace un miembro remarcable de la
cadena es que es un gas noble. Esto significa que no
reacciona quımicamente y, por tanto, permanece en la
atmósfera una vez liberado. Hace mucho tiempo que este gas es
tristemente conocido
por alcanzar peligrosas concentraciones en las minas de uranio.
La solución a la excesiva concentración de radon tambien
se conoce desde hace tiempo: la ventilación es la única
forma de eliminarlo.
con semivida relativamente corta (3.8 d)
y la caracterıstica que lo hace un miembro remarcable de la
cadena es que es un gas noble. Esto significa que no
reacciona quımicamente y, por tanto, permanece en la
atmósfera una vez liberado. Hace mucho tiempo que este gas es
tristemente conocido
por alcanzar peligrosas concentraciones en las minas de uranio.
La solución a la excesiva concentración de radon tambien
se conoce desde hace tiempo: la ventilación es la única
forma de eliminarlo.
Puesto que es un gas que está entrelazado en una cadena secuencial de materiales sólidos no volátiles, el radon puede dar mobilidad a los isótopos en el segmento de la cadena que le sigue. Y aquı es donde reside el mayor problema. Un esquema simplificado de este proceso se muestra en la figura 3.
La secuencia inicial de desintegración en la cadena está compuesta
únicamente por elementos sólidos, hasta el radio-226.
Son metales pesados y se encuentran generalmente en
formaciones de rocas, donde permanecen durante años hasta que
el ![]() Ra (radio-226) se desintegra en
Ra (radio-226) se desintegra en ![]() Rn (radon-222).
Desde este momento el material es volátil y puede difundirse
en la atmósfera por cualquier fisura en la roca.
Rn (radon-222).
Desde este momento el material es volátil y puede difundirse
en la atmósfera por cualquier fisura en la roca.
Por sı sólo, el Rn no crearıa un gran problema, ya que
es un gas noble y no se deposita en los tejidos.
Puesto que está presente en la atmósfera, puede ser inhalado,
pero como no reacciona qu´ımicamente, la mayor
parte será exalada de nuevo en cuestión de segundos o minutos.
La probabilidad de que se desintegre en este intervalo de tiempo
es pequeña. No obstante, el siguiente miembro de la cadena,
el Polonio-218, es sólido de nuevo. Por lo tanto, puede depositarse,
reaccionar quımicamente y permanecer localizado. Más aún,
el ![]() Po es sólo el primer miembro de una secuencia
de desintegración muy rápida (
Po es sólo el primer miembro de una secuencia
de desintegración muy rápida (![]() Po,
Po, ![]() Pb,
Pb, ![]() Bi,
Bi,
![]() Po,
Po, ![]() Pb) que emitirá numerosas partıculas cargadas
muy peligrosas. Con el
Pb) que emitirá numerosas partıculas cargadas
muy peligrosas. Con el ![]() Pb, con semivida de 22.3 años,
hay una pausa relativa en la cadena, por lo que la
concentración de
Pb, con semivida de 22.3 años,
hay una pausa relativa en la cadena, por lo que la
concentración de ![]() Pb se incrementa paulatinamente.
Esto explica la importancia de este isótopo, que ya apuntamos,
por ejemplo, cuando discutimos los efectos de la radiación en los
fumadores. Ahora no es difıcil entender cómo llega el
plomo a formar parte del tabaco: el Rn de la atmósfera
se desintegra produciendo el
Pb se incrementa paulatinamente.
Esto explica la importancia de este isótopo, que ya apuntamos,
por ejemplo, cuando discutimos los efectos de la radiación en los
fumadores. Ahora no es difıcil entender cómo llega el
plomo a formar parte del tabaco: el Rn de la atmósfera
se desintegra produciendo el ![]() Pb, que se deposita en las hojas
de la planta del tabaco cuando está creciendo. Puesto que este
isótopo tiene una semivida de 22.3 años, existe una probabilidad
alta de que se deposite en los pulmones de un fumador.
Pb, que se deposita en las hojas
de la planta del tabaco cuando está creciendo. Puesto que este
isótopo tiene una semivida de 22.3 años, existe una probabilidad
alta de que se deposite en los pulmones de un fumador.
Ya podemos explicar también en qué consiste el problema del radon en las viviendas y por qué esta fuente de radiación puede ser tan variable. La fuente última de Rn es el subsuelo. No obstante, las condiciones del suelo, especialmente la permeabilidad, pueden variar considerablemente. Los edificios construidos sobre terrenos permeables o formaciones rocosas con fisuras pueden servir como carpas para el radon que se difunde hacia arriba. Por tanto, el radon que, en condiciones normales, se difundirıa en la atmósfera, queda enclaustrado en el interior de los edificios.
Ejemplo El sótano de una casa tiene un volumen de 160 m. A través del suelo se filtra radon a razón de 40 pCi de
Rn por hora. Calcular la concentración y actividad asintótica por unidad de volumen del radon (
) en este sótano, suponiendo que no hay ventilación.
Seael número de átomos de Rn y
el número de átomos de radon que se filtran en el sótano por unidad de tiempo. Se tiene
de donde,
Multiplicando por,
obtenemos en el primer miembro una derivada exacta:
Integrando los dos miembros entre 0 y:
Despejandoy suponiendo que inicialmente
,
El número asintótico de átomos se obtiene tomando el lımite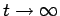
Por tanto, basta que calculemosy
. A partir de la semivida
d, obtenemos la constante de desintegración
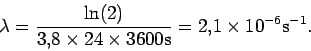
Por otra parte, sabemos que el Rn se filtra a razon de
Ahora bien, dado que la actividad es, el número de átomos de Rn con una actividad de
Bq es
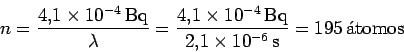
Por lo tanto,y el número asintótico de átomos será
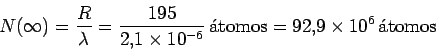
La concentraci'on asintótica será de
La actividad asintótica por unidad de volumen será entonces
La concentración normal de ![]() Rn en la atmósfera es de
Rn en la atmósfera es de
![]() a 4 pCi
a 4 pCi![]() m
m![]() y, por lo tanto, la concentración
en el sótano es apreciablemente alta.
Supongamos ahora que hay ventilación que cambia el aire
una vez al dia.
y, por lo tanto, la concentración
en el sótano es apreciablemente alta.
Supongamos ahora que hay ventilación que cambia el aire
una vez al dia.
Ejemplo Repetir los cálculos del problema anterior, suponiendo que hay un sistema de ventilación que cambia el aire del sótano una vez al dıa.
Suponemos que el sistema de ventilación funciona continuamente. Si inicialmente hayatomos que al cabo de un dıa son completamente eliminados, en un intervalo de tiempo d
el número de átomos eliminados será
Esto quiere decir que La tasa de disminución de Rn debido a la ventilación está dada pory, por tanto, el efecto de la ventilación puede tenerse en cuenta sumando a su constante de desintegración la asociada a la ventilación:
El número asintótico de átomos será
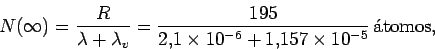
es decir,
La concentraci´on asintótica será de
La actividad asintótica por unidad de volumen será entonces